การหาสภาวะที่เหมาะสมในการสกัดมิโมซีนโดยใช้การออกแบบการทดลอง
คำสำคัญ:
มิโมซีน, การออกแบบการทดลอง, วิธีบ็อกซ์เบห์นเคน, วิธีพื้นผิวตอบสนอง, ตัวทำละลายธรรมชาติบทคัดย่อ
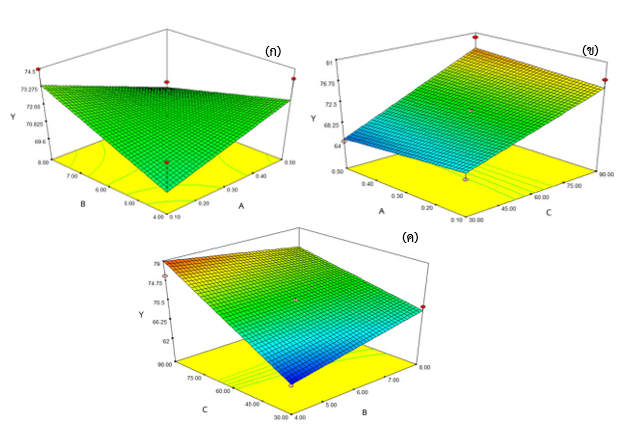
มิโมซีน (Mimosine) เป็นกรดอะมิโนอิสระที่พบได้มากกระถิน (Leucaena leucocephala) ในงานวิจัยนี้งมีวัตถุประสงค์เพื่อศึกษาสภาวะที่เหมาะสมในการสกัดมิโมซีนจากยอดอ่อนใบกระถินด้วยตัวทำละลาย NADES (ซึ่งในงานวิจัยนี้ใช้สารละลายโคลีนคลอไรด์ในน้ำ) โดยวิธีการแช่สกัด ทำการศึกษาปัจจัยที่ส่งผลต่อการสกัดมิโมซีนจากยอดอ่อนใบกระถิน คือ ความเข้มข้นของตัวทำละลาย NADES pH เวลา ปริมาตรตัวทำละลาย NADES และอุณหภูมิ ออกแบบการทดลองโดยวิธีบ็อกซ์เบห์นเคน (Box–Behnken designs) ร่วมกับวิธีพื้นผิวตอบสนอง (Response Surface Methodology) วิเคราะห์ปริมาณสารด้วยเทคนิคยูวีวิสซิเบิลสเปกโตรสโกปี ที่ความยาวคลื่น 282
นาโนเมตร ผลการศึกษาพบว่า ที่ความเข้มข้นของตัวทำละลาย NADES 0.50 โมแลล pH 6 และเวลาในการสกัด 90 นาที จะให้ปริมาณมิโมซีนสูงสุด 80.03±2.29 มิลลิกรัมต่อกรัม และที่ปริมาตรตัวทำละลาย NADES 50.00 มิลลิลิตร pH 7 และ อุณหภูมิ 90 องศาเซลเซียส จะให้ปริมาณมิโมซีนสูงสุด 76.46±0.95 มิลลิกรัมต่อกรัม จากการศึกษาพบว่าการสกัดสารมิโมซีนจากยอดอ่อนใบกระถินด้วยตัวทำละลาย NADES ช่วยในการเพิ่มความสามารถในการสกัดมิโมซีนได้มากกว่าการสกัดแบบธรรมดาที่สกัดด้วยน้ำร้อน
เอกสารอ้างอิง
ประไพศรี สุทัศน์ ณ อยุธยา และพงศ์ชนัน เหลืองไพบูลย์. (2551). การออกแบบและวิเคราะห์การทดลอง (Design and Analysis of Experiments). สมุทรปราการ: สำนักพิมพ์ท้อป.
Anitha, R., Jayavelu, S., & Murugesan, K. (2005). Antidermatophytic and bacterial activity of mimosine. Phytotherapy Research, 19(11), pp.992-993. https://doi.org/10.1002/ptr.1761
Brewbaker, J. L., & Hylin, J. W. (1965). Variation in mimosine content among Leucaena species and related Mimosaceae. Crop Science, 5(4), pp.348-351. https://doi.org/10.2135/cropsci1965.0011183X000500040019x
Champanerkar, P.A., Vaidya, V.V., Shailajan, S. & Menon, S.N. (2010). A sensitive, rapid and validated liquid chromatography ? tandem mass spectrometry (LC-MS-MS) method for determination of Mimosine in Mimosa pudica Linn. Natural Science, 2(7), pp.689-695. https://doi.org/10.4236/ns.2010.27088
Chang, H. C., Liu, L. T., Hung, W. C., & Wang, C. J. (1999). Mimosine inhibits proliferation of hepatoma cells by inducing apoptosis through mitochondrial stress. Toxicology and Applied Pharmacology, 157(1), pp.52-60. https://doi.org/10.1006/taap.1999.8677
Dai, Y., Gold, B., Vishwanatha, J. K., & Rhode, S. L. (1994). Mimosine inhibits viral DNA synthesis through ribonucleotide reductase. Virology, 205(1), pp.210-216. https://doi.org/10.1006/viro.1994.1636
Dai, Y., van Spronsen, J., Witkamp, G.-J., Verpoorte, R., & Choi, Y. H. (2013). Natural deep eutectic solvents as new potential media for green technology. Analytica Chimica Acta, 766, pp.61-68. https://doi.org/10.1016/j.aca.2012.12.019
Hallak, M., Vazana, L., Shpilberg, O., Levy, I., Mazar, J., & Nathan, I. (2008). A molecular mechanism for mimosine-induced apoptosis involving oxidative stress and mitochondrial activation. Apoptosis, 13(1), pp.147-155. https://doi.org/10.1007/s10495-007-0156-7
Honda, M. D. H., & Borthakur, D. (2019). Mimosine concentration in Leucaena leucocephala under various environmental conditions. Tropical Grasslands-Forrajes Tropicales, 7(2), pp.164-172. https://doi.org/10.17138/TGFT(7)164-172
Ilham, Z., Hamidon, H., & Rosji, N.A. (2015). Extraction and quantification of toxic compound mimosine from biomass residues of Leucaena leucocephala. Procedia Chemistry, 16, pp.164-170. https://doi.org/10.1016/j.proche.2015.12.029
Kubota, S., Fukumoto, Y., Ishibashi, K., Soeda, S., Kubota, S., Yuki, R., Nakayama, Y., Aoyama, K., Yamaguchi, N., & Yamaguchi, N. (2014). Activation of the prereplication complex is blocked by mimosine through reactive oxygen species-activated ataxia telangiectasia mutated (ATM) protein without DNA damage. Journal of Biological Chemistry, 289(9), pp.5730-5746. https://doi.org/10.1074/jbc.M113.546655
Lalitha, K. & Kulothungan, S. R. (2004). Determination of mimosine by a sensitive indirect spectrophotometric method. Talanta, 63(3), pp.635-640. https://doi.org/10.1016/j.talanta.2003.12.006
Méchali, M. (2010). Eukaryotic DNA replication origins: Many choices for appropriate answers. Nature Reviews Molecular Cell Biology, 11(10), pp.728-738. https://doi.org/10.1038/nrm2976
Montgomery, D. C. (2017). Design and Analysis of Experiments (9th ed.). New York: John Wiley & Sons.
Nair, L. S., Menon, S. N., Shailajan, S., Baing, M. M., & Sane, R. T. (2007). Reverse phase high performance thin layer chromatographic quantification of mimosine from whole plant of Mimosa pudica Linn. Journal of Planar Chromatography – Modern TLC, 20(1), pp.49-51. https://doi.org/10.1556/jpc.20.2007.1.7
Nguyen, B. C. Q., Chompoo, J., & Tawata, S. (2015). Insecticidal and Nematicidal Activities of Novel Mimosine Derivatives. Molecules, 20(9), pp.16741-16756. https://doi.org/10.3390/molecules200916741
Nguyen, V. H., & Tawata, S. (2016). Mimosine: Biosynthesis and biological activities. Journal of Agricultural and Food Chemistry, 64(22), pp.4237-4245. https://doi.org/10.1002/ptr.5636
Puchala, R., Davis, J. J., & Sahlu, T. (1996). Determination of mimosine and 3,4-dihydroxypyridine in milk and plasma of goats. Journal of Agricultural and Food Chemistry, 685(2), pp.375-378.https://doi.org/10.1016/S0378-4347(96)00221-6
Ramesh, S., Venkatesan, G., Karthikeyan, K., Sundari, C. K., & Chandran, C. (2021). Studies on the active components of sensitive plant Mimosa pudica L. (Mimosaceae). Plant Cell Biotechnology and Molecular Biology, 22(57&58), pp.88-96.
Renz J. (1936). Uber das mimosin. Zeitschrift fur Physiologische Chemie, 244, pp.153-158.
Sahid, I., Ishak, M. S., Bajrai, F. S., Jansar, K. M., & Yusoff, N. (2017). Quantification and herbicidal activity of mimosine from Leucaena leucocephala (Lam.) de Wit. Transactions on Science and Technology, 4(2), pp.62-67.
Tangendjaja, B. & Wills, R. B. H. (1980). Analysis of mimosine and 3-hydroxy-4(1H)-pyridone by high- performance liquid chromatography, Journal of Chromatography A . 202(2), pp.317-318. https://doi.org/10.1016/S0021-9673(00)81746-X
Watson, P. A., Hanauske-Abel, H. H., Fiint, A. & Lalande, M. (1991). Mimosine arrests cell cycle progression at the G1-Sphase border. Cytometry, 12(3), pp.242–246. https://doi.org/10.1002/cyto.990120306
Wu, C., Yuan, H., Jia G., Wang, Z. & Wu, X. (2011). Determination of Mimosine and 2,3-Dihydroxypyridine in Leucaena leucocephala by Reversed Phase High-Performance Liquid Chromatography. Applied Mechanics and Materials, 140, pp.296-301. https://doi.org/10.4028/www.scientific.net/AMM.140.296
ดาวน์โหลด
เผยแพร่แล้ว
รูปแบบการอ้างอิง
ฉบับ
ประเภทบทความ
สัญญาอนุญาต
ลิขสิทธิ์ (c) 2025 วารสารวิจัย วิทยาศาสตร์และเทคโนโลยี มหาวิทยาลัยราชภัฏนครราชสีมา

อนุญาตภายใต้เงื่อนไข Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License.
เนื้อหาและข้อมูลในบทความที่ลงตีพิมพ์ในวารสารวิจัย วิทยาศาสตร์และเทคโนโลยี มหาวิทยาลัยราชภัฏนครราชสีมา ถือเป็นข้อคิดเห็นและความรับผิดชอบของผู้เขียนบทความโดยตรงซึ่งกองบรรณาธิการวารสาร ไม่จำเป็นต้องเห็นด้วย หรือร่วมรับผิดชอบใด ๆ
บทความ ข้อมูล เนื้อหา รูปภาพ ฯลฯ ที่ได้รับการตีพิมพ์ในวารสารวิจัย วิทยาศาสตร์และเทคโนโลยี มหาวิทยาลัยราชภัฏนครราชสีมา ถือเป็นลิขสิทธิ์ของวารสารวิจัย วิทยาศาสตร์และเทคโนโลยี มหาวิทยาลัยราชภัฏนครราชสีมา หากบุคคลหรือหน่วยงานใดต้องการนำทั้งหมดหรือส่วนหนึ่งส่วนใดไปเผยแพร่ต่อหรือเพื่อกระทำการใด ๆ จะต้องได้รับอนุญาตเป็นลายลักอักษรจากวารสารวิจัย วิทยาศาสตร์และเทคโนโลยี มหาวิทยาลัยราชภัฏนครราชสีมา ก่อนเท่านั้น


